高中物理知识点:氢原子的能级
逍遥右脑 2016-02-19 08:44
氢原子的能级:
1、氢原子的能级图 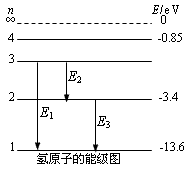
2、光子的发射和吸收
①原子处于基态时最稳定,处于较高能级时会自发地向低能级跃迁,经过一次或几次跃迁到达基态,跃迁时以光子的形式放出能量。
②原子在始末两个能级Em和En(m>n)间跃迁时发射光子的频率为ν,其大小可由下式决定:hυ=Em-En。
③如果原子吸收一定频率的光子,原子得到能量后则从低能级向高能级跃迁。
④原子处于第n能级时,可能观测到的不同波长种类N为:![]() 。
。
⑤原子的能量包括电子的动能和电势能(电势能为电子和原子共有)即:原子的能量En=EKn+EPn。轨道越低,电子的动能越大,但势能更小,原子的能量变小。
电子的动能:![]() ,r越小,EK越大。
,r越小,EK越大。
氢原子的能级及相关物理量:
在氢原子中,电子围绕原子核运动,如将电子的运动看做轨道半径为r的圆周运动,则原子核与电子之间的库仑力提供电子做匀速圆周运动所需的向心力,那么由库仑定律和牛顿第二定律,有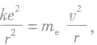 ,则
,则
①电子运动速率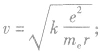
②电子的动能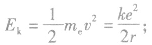
③电子运动周期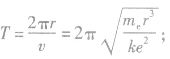
④电子在半径为r的轨道上所具有的电势能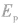
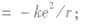
⑤等效电流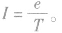 由以上各式可见,电子绕核运动的轨道半径越大,电子的运行速率越小,动能越小,电子运动的周期越大.在各轨道上具有的电视能越大。
由以上各式可见,电子绕核运动的轨道半径越大,电子的运行速率越小,动能越小,电子运动的周期越大.在各轨道上具有的电视能越大。
原子跃迁时光谱线条数的确定方法:
1.直接跃迁与间接跃迁
原子从一种能量状态跃迁到另一种能量状态时,有时可能是直接跃迁,有时可能是间接跃迁,两种情况辐射(或吸收)光子的频率可能不同。
2.一群原子和一个原子
氧原子核外只有一个电子,这个电子在某个时刻只能处在某一个可能的轨道上,在某段时间内,由某一轨道跃迁到另一个轨道时,可能的情况只有一种,但是如果容器中盛有大量的氢原子,这些原子的核外电子跃迁时就会有各种情况出现了。
3.一群氢原子处于量子数为n的激发态时,可能辐射的光谱线条数
如果氢原子处于高能级,对应量子数为n,则就有可能向量子数为(n一1),(n一2),(n一3)…1诸能级跃迁,共可形成(n一1)条谱线,而跃迁至量子数为(n一 1)的氢原子又可向(n一2),(n一3)…1诸能级跃迁,共可形成(n一2)条谱线。同理,还可以形成(n一3),(n 一4)…1条谱线。将以上分析结果归纳求和,则从量子数为n对应的能级向低能级(n―1),(n一2)…1跃迁可形成的谱线总条数为(n一1)+(n一2)+(n一3)+ …+1=n(n一1)/2。数学表示为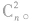
4.一个氢原子处于量子数为n的激发态时,可能辐射的光谱线条数
对于处于量子数为n的一个氢原子,它可能发生直接跃迁,只放出一个光子,也可能先跃迁到某个中间能级上,再跃迁回基态而放出两个光子,也可能逐级跃迁,即先跃迁到n一1能级上,再跃迁到n一2能级上, ……,最后回到基态上,共放出n―1个光子。即一个氢原子在发生能级跃迁时,最少放出一个光子,最多可放出n一1个光子。
利用能量守恒及氢原子能级特征解决跃迁电离等问题的方法:
在原子的跃迁及电离等过程中,总能量仍是守恒的。原子被激发时,原子的始末能级差值等于所吸收的能量,即入射光子的全部能量或者入射粒子的全部或部分能量;原子被电离时,电离能等于原子被电离前所处能级的绝对值,原子所吸收的能量等于原子电离能与电离后电离出的电子的动能之和;辐射时辐射出的光子的能量等于原子的始末能级差。氢原子的能级 F 关系为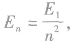 ,第n能级与量子数n2成反比,导致相邻两能级间的能量差不相等,量子数n越大,相邻能级差越小,且第n能级与第n一1能级的差比第n能级与无穷远处的能级差大,即
,第n能级与量子数n2成反比,导致相邻两能级间的能量差不相等,量子数n越大,相邻能级差越小,且第n能级与第n一1能级的差比第n能级与无穷远处的能级差大,即 另外,能级差的大小
另外,能级差的大小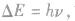 故也可利用光子能量来判定能级差大小。
故也可利用光子能量来判定能级差大小。
跃迁与电离:
激发的方式:
相关高中物理知识点:玻尔的原子理论
玻尔的原子理论:
| 经典理论的困难 | 原子的稳定性 | 电子做加速运动应该辐射电磁波,逐渐减小能量和轨道半径,最终落入原子核,原子是不稳定的,与事实不符 |
| 原子光谱的分立性 | 电子绕核运行辐射频率应等于电子绕核运行频率,由于运行轨道的减小,辐射电磁波频率应不断变化而形成连续光谱,这与原子光谱一明线光谱不符(固定的若干种频率) | |
| 玻尔理论基础 | 实验基础 | 氢原子光谱的分立特征 |
| 理论基础 | 普朗克关于黑体辐射的量子论与爱因斯坦的光子说 | |
| 波尔理论内容 | 量子化假设 | ①电子的轨道是量子化的。电子运行轨道的半径不是任意的,只有半径的大小符合一定条件的轨道才是可能的。电子在这些轨道上绕核的转动是稳定的,不产生电磁辐射 ②原子的能量是量子化的。这些量子化的能量值叫做能级。原子中这些具有确定能量的稳定状态称为定态。能量最低的状态叫做基态,其他的状态叫做激发态 |
| 频率条件 | 当电子从能量较高的定态轨道(Em)跃迁到能量较低的定态轨道(En)时,会放出能量为hv的光子,这个光子的能量由前后两个能级的能量差决定,即hv=Em一En | |
| 对光谱的解释 | 原子光谱的分立性 | 通常情况下,原子处于基态,基态是稳定的,处于激发态的原子是不稳定的。原子从高能态向低能态跃迁时放出的光子的能量等于前后两个能级之差。由于原子的能级是分立的,所以放出的光子的能量也是分立的。因此原子的发射光谱只有一些分立的亮线 |
| 特征谱线 | 由于不同的原子具有不同的结构,能级各不相同,因此辐射(或吸收)的光子频率也不同,这就是不同元素的原子具有不同的特征谱线的原因 | |
| 氢原子光谱线系 | 玻尔理论不但成功地解释了氢光谱的巴耳末系,而且对当时已发现的氢光谱的另一线系――帕邢系(在近红外区)也能很好地解释。它是电子从n=4、5、6等能级向n=3 能级跃迁时辐射出来的。此外,玻尔理论还预言了当时尚未发现的氢原子的其他光谱线系,这些线系后来相继被发现,也都跟玻尔理论的预言相符 |
玻尔的原子理论的成功与局限:
玻尔的原子理论第一次将量子观引入原子领域,提出定态和跃迁的概念,成功地解释了氢原子光谱规律,但玻尔引入的量子化观点并不完善。在量子力学中,核外电子并没有确定的轨道,玻尔的电子轨道只不过是电子出现概率较大的地方。把电子的概率分布用图像表示时,用小黑点的稠密程度代表概率的大小,其结果如同电子在原子核周围形成的云雾,称为“电子云
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 lxy@jiyifa.cn 举报,一经查实,本站将立刻删除。